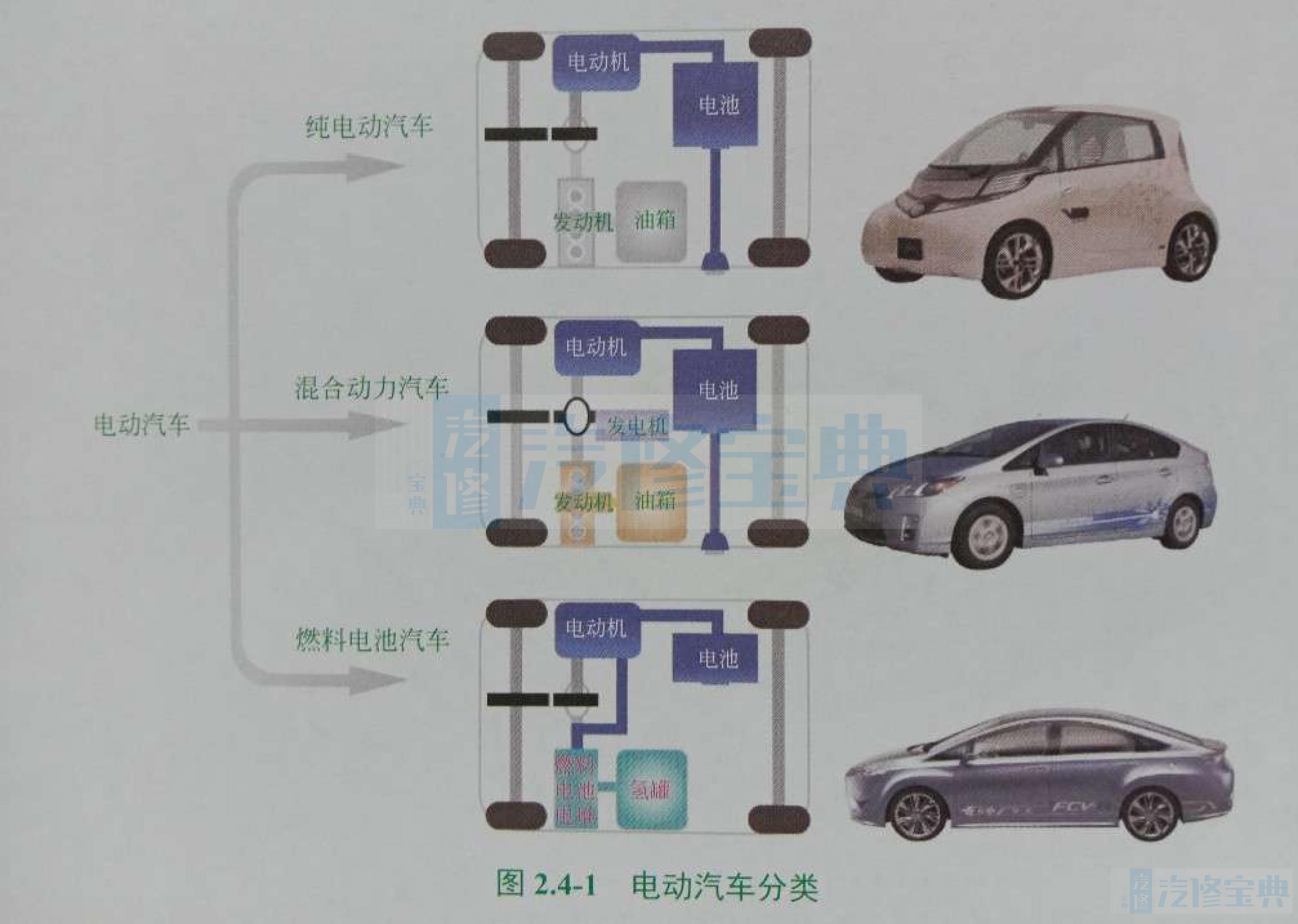
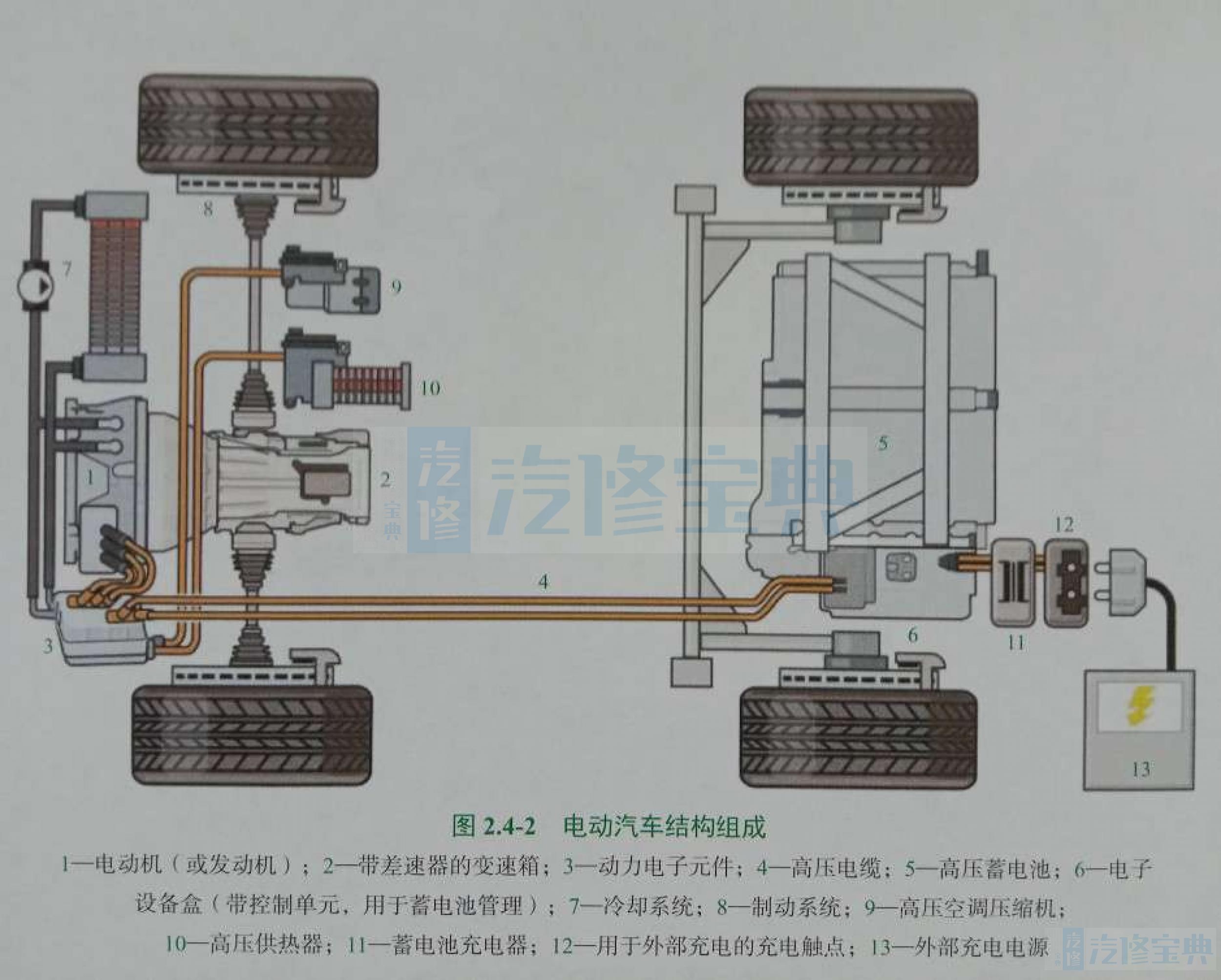
电动汽车包括纯电动汽车、燃料电池汽车和插电式(含增程式)混合动力汽车,都是以电能驱动车辆行驶,使用的是动力电池。电动汽车分类见图2.4-1,电动汽车结构组成见图2.4-2。
动力电池(图2.4-3)是电动汽车的心脏。动力电池多以钴酸锂、锰酸锂或镍酸锂等化合物为正极,以可嵌入锂离子的碳材料为负极,使用有机电解质。动力电池总成安装在车体下部,动力电池的组成部件包括各模组总成、采集系统、电池控制单元、电池高压分配单元、维修开关等部件。电动汽车电池组由多个电池串联叠置组成。一个典型的电池组含90多个电池,对充电到4.2V的锂离子电池而言,这样的电池组可产生超过400V的总电压。
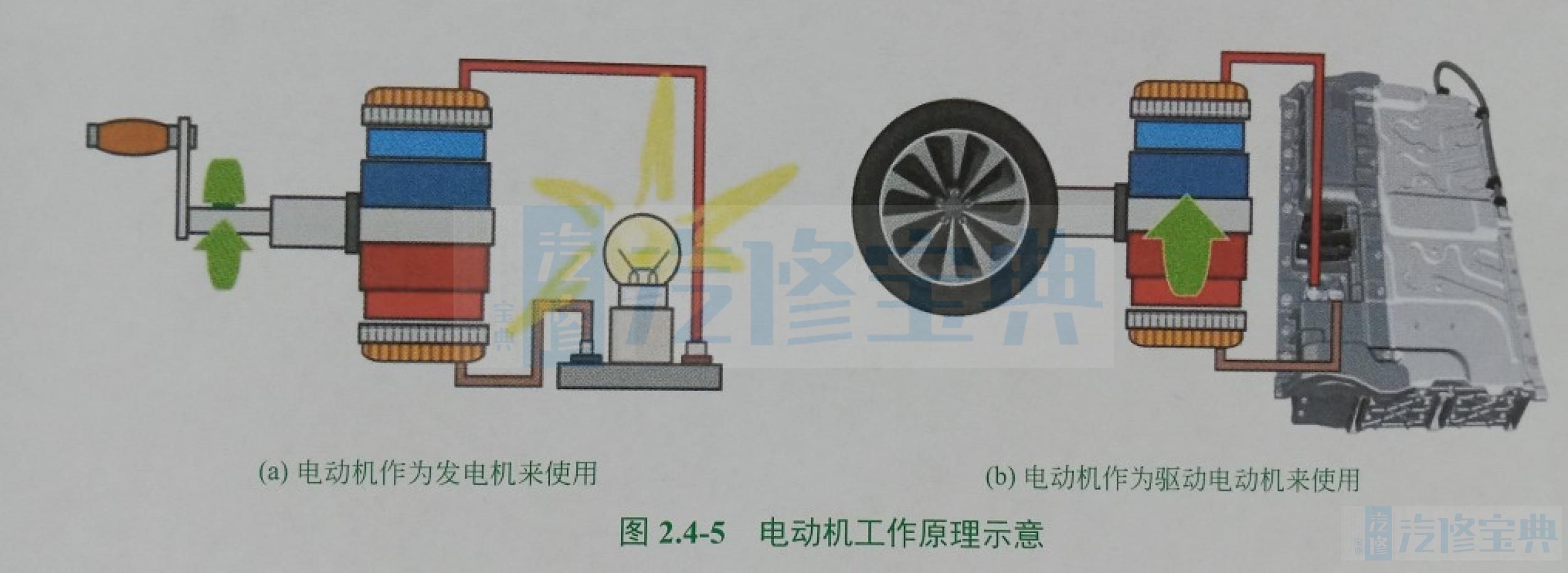
理论而言,任何电动机都可被用作交流发电机。当机械装置驱动电动机时,它将作为交流发电机供电;当向电动机供给电流时,它作为驱动装置运行。
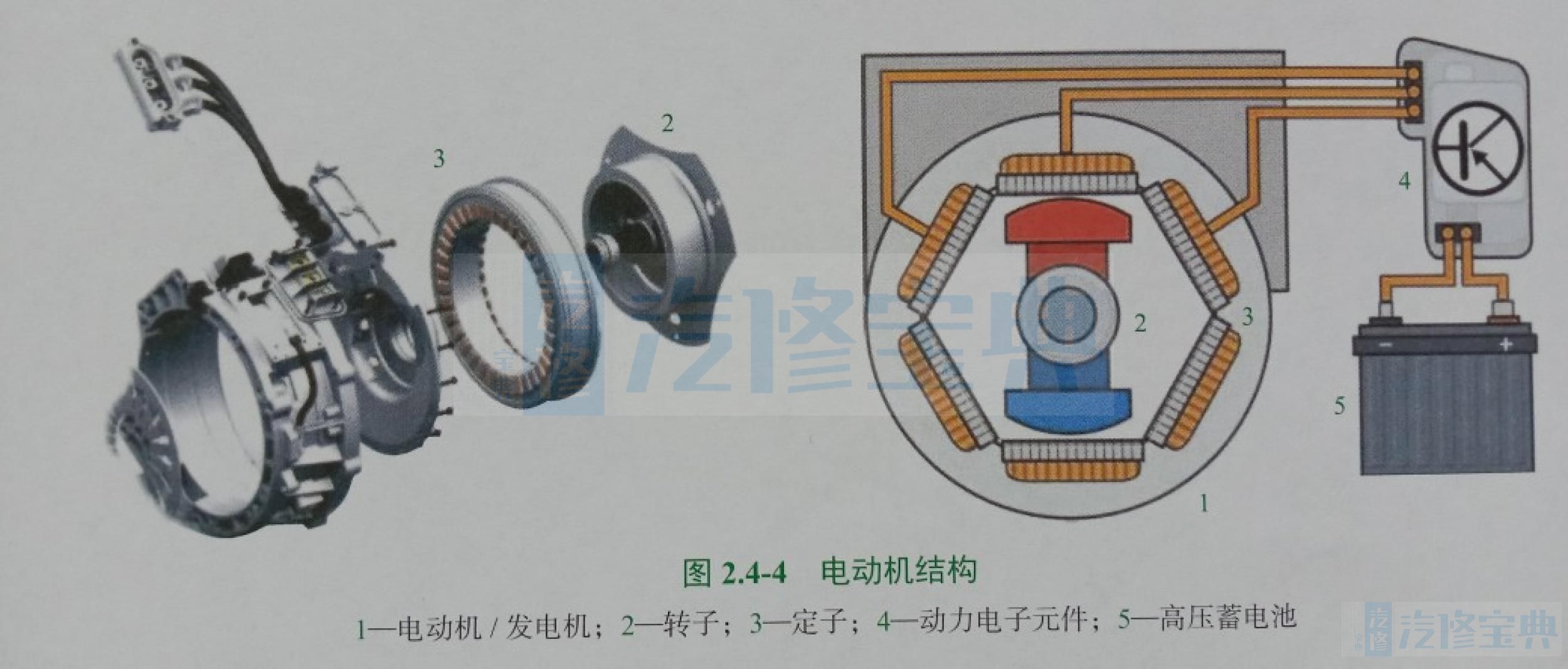
三相电动机经常用作电动机/发电机。三相电动机由三相交流电供能。它与环绕转子的三条线圈协同工作并形成定子,三条线圈分别连接至三相电动机的一相。在该同步电动机中,若干对永磁体位于转子上方。由于对三相线圈连续供电,因此它们会产生一个旋转电磁场,从而在使用电动机/发电机驱动车辆时使转子旋转。
当电动机/发电机用作交流发电机时,转子的运动会使线圈产生三相交流电压,并转换成动力电子元件中高压蓄电池的直接电压。通常情况下,车辆会使用所谓的“同步电动机”。
就此而论,“同步性”即“同步运行”,指的是定子线圈中能量场的转速与带永磁体转子转速的比率。
同步电动机与非同步电动机相比的优势在于,同步电动机在自动化应用时可以更精确控制电动机。
电动机结构、工作原理如图2.4-4和图2.4-5所示。
一、纯电动汽车。
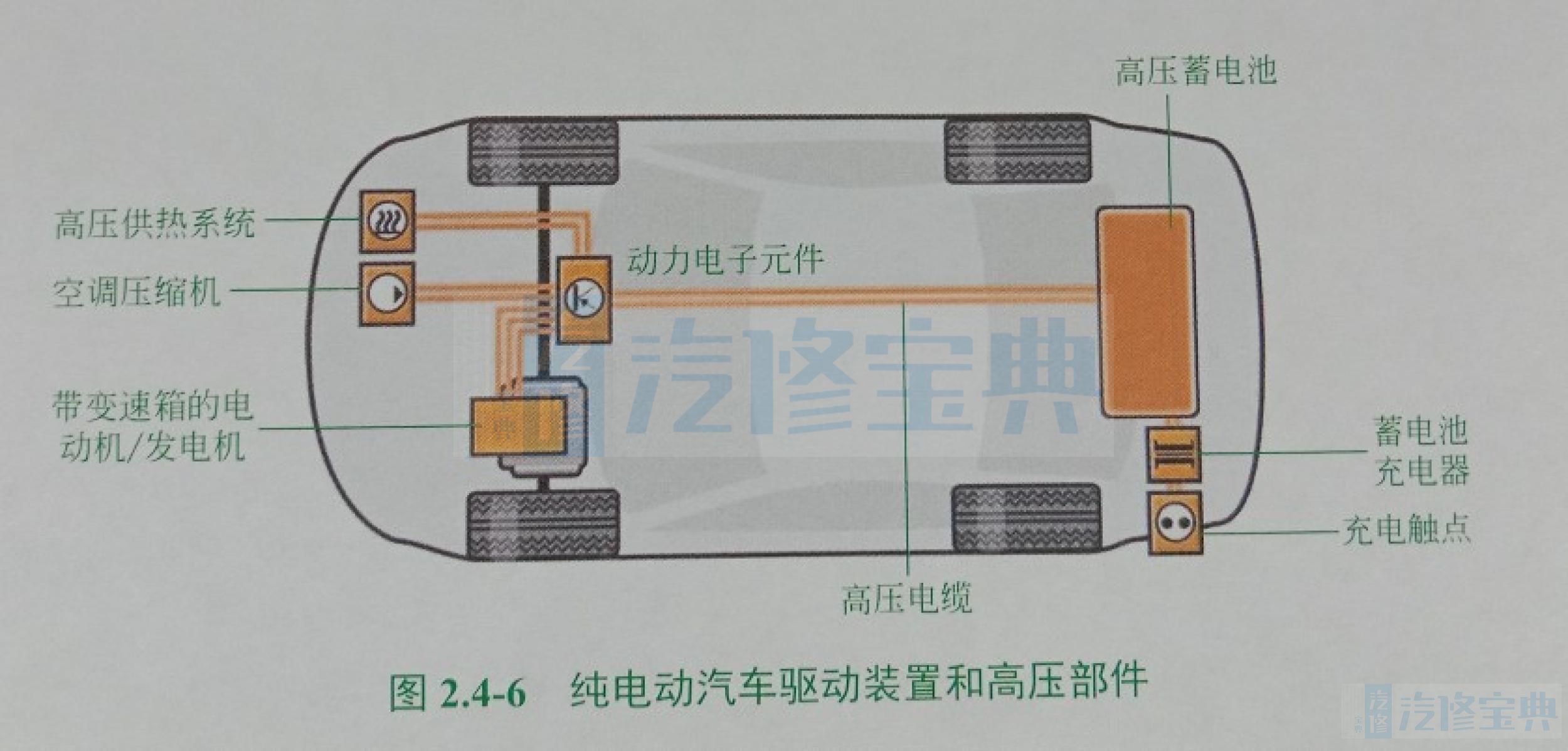
纯电动汽车是指以车载电源为动力,用电动机驱动车轮行驶的汽车,它完全由可充电电池提供动力源,其驱动装置和高压部件如图2.4-6所示。
二、混合动力汽车。
1.总体结构。
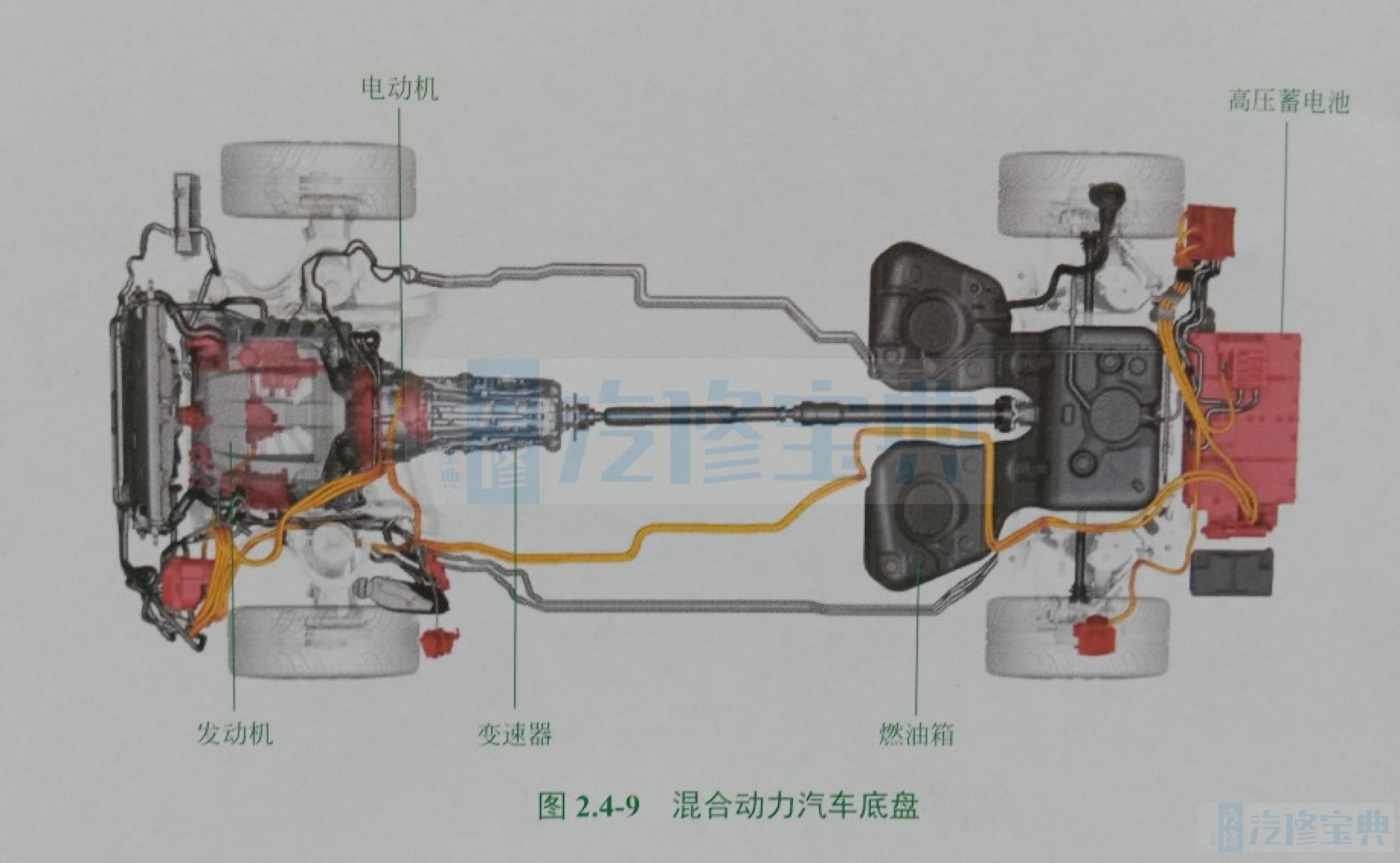
混合动力汽车一般是指油电混合动力汽车,即采用传统的汽油发动机或者柴油发动机和电动机作为动力源,如图2.4-7~图2.4- 9所示。
2.混合动力汽车类型。
根据混合动力驱动的联结方式,一般把混合动力汽车分为三类。
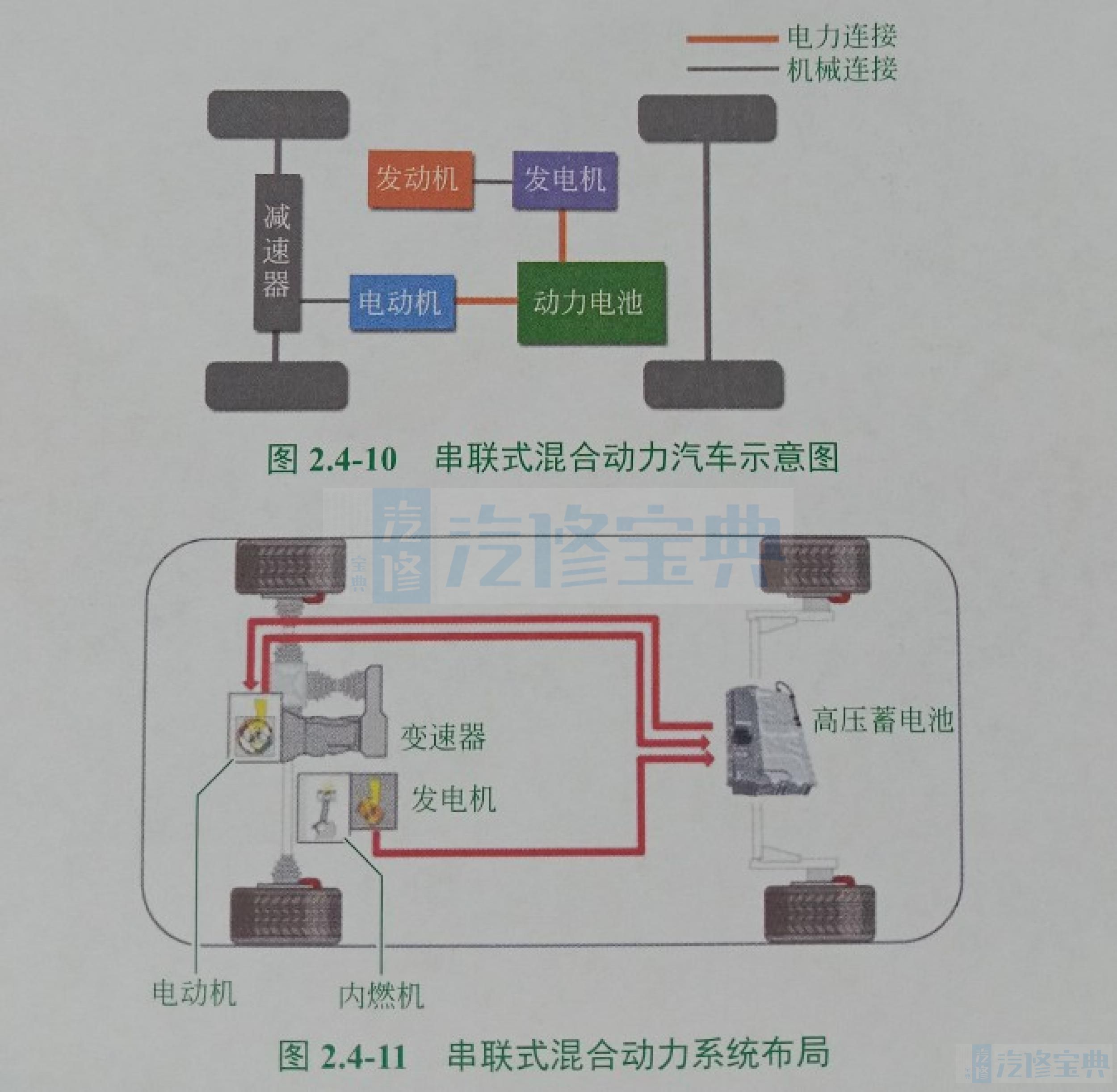
(1)串联式混合动力汽车(SHEV)。串联式混合动力汽车主要由发动机、发电机、驱动电动机三大动力总成用串联方式组成HEV的动力系统。串联混动结构的动力来源于电动机,发动机只能驱动发电机发电,并不能直接驱动车辆行驶。因此,串联结构中电动机功率一般要大于发动机功率,这样才能满足车辆的行驶需求(图2.4-10和图2.4-11)。高压蓄电池也就是动力电池。
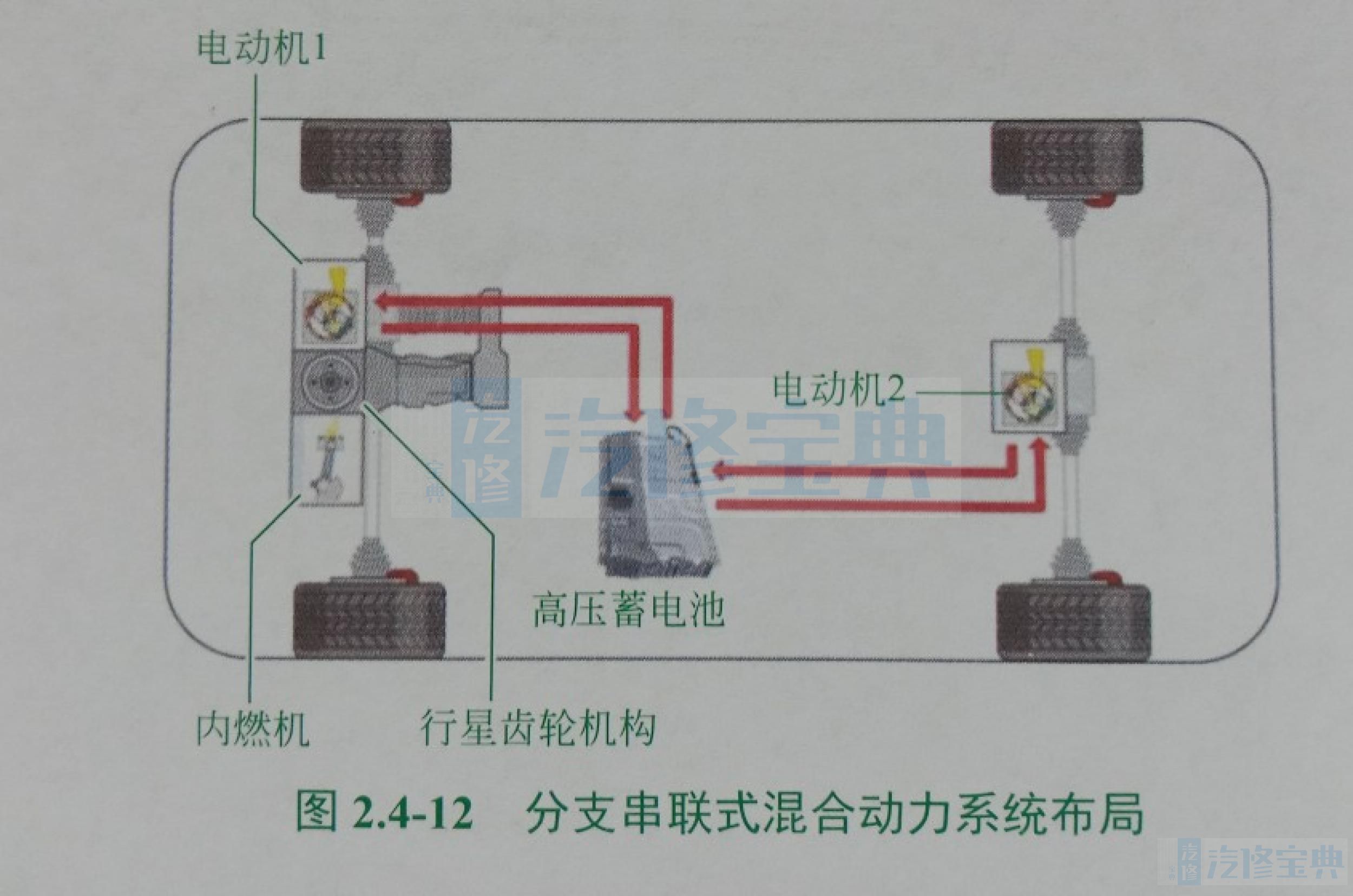
还有一种分支串联式混合动力系统,就是把分支式混合动力系统和串联式混合动力系统综合在一起(图2.4-12)。该系统有一个发动机和两个电动机。发动机和电动机1装在前桥上,电动机2装在后桥上。这种结构用于四轮驱动车。发动机和电动机1可以通过行星齿轮机构来驱动车辆变速器。
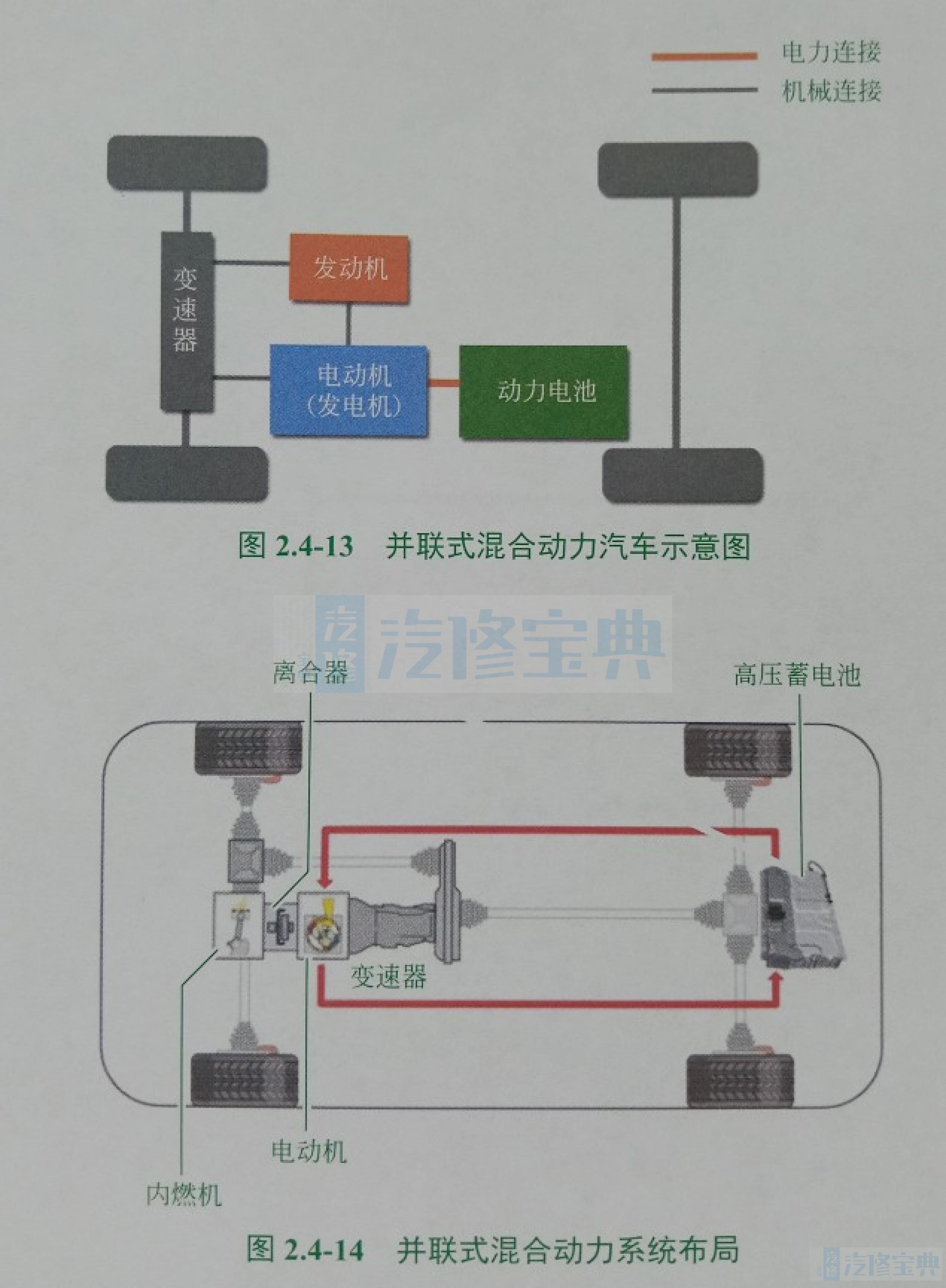
(2)并联式混合动力汽车(PHEV)。并联式混合动力汽车的发动机和发电机都是动力总成,两大动力总成的功率可以互相叠加输出,也可以单独输出。
并联式混合动力汽车靠发动机或者电动机,或发动机和电动机共同驱动(图2.4-13)。
并联结构保留了变速器,因此,通俗地讲,并联混动结构即普通汽车+电动机=并联(图2.4-14)。
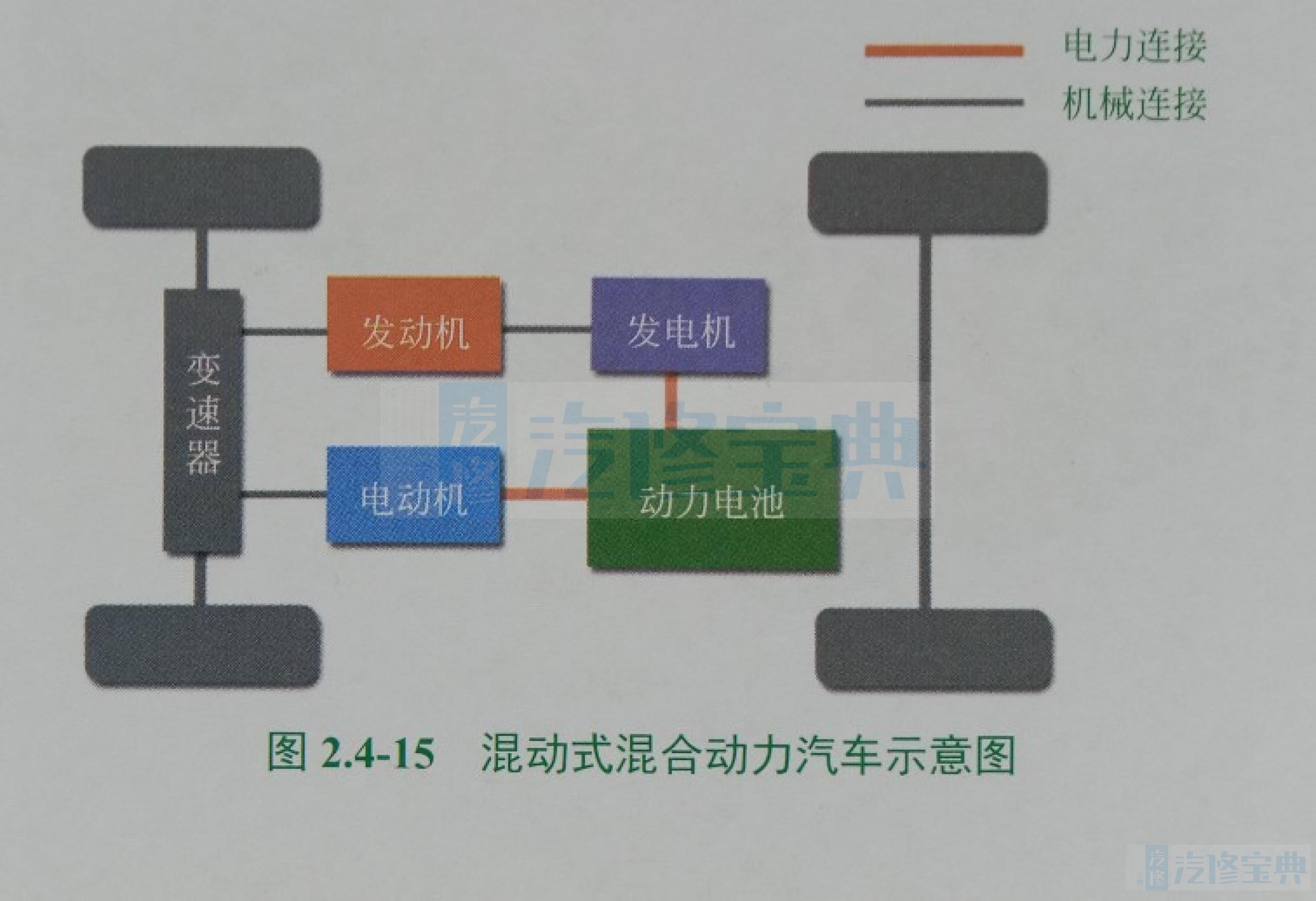
(3)混动式混合动力汽车( PSHEV)。混动式混合动力汽车是综合了串联式和并联式的结构而组成的电动汽车,主要由发动机、电动机-发电机和驱动电机三大动力总成组成。
在发动机和电动机协同驱动汽车行驶的同时,发动机还能带动发电机为电池充电,不再像并联结构中单一电动机需要身兼二职,并且理论上它能够实现发动机带动发电机发电电动机驱动汽车的模式(图2.4-15)。当然,两个动力单元也能够单独驱动车辆。
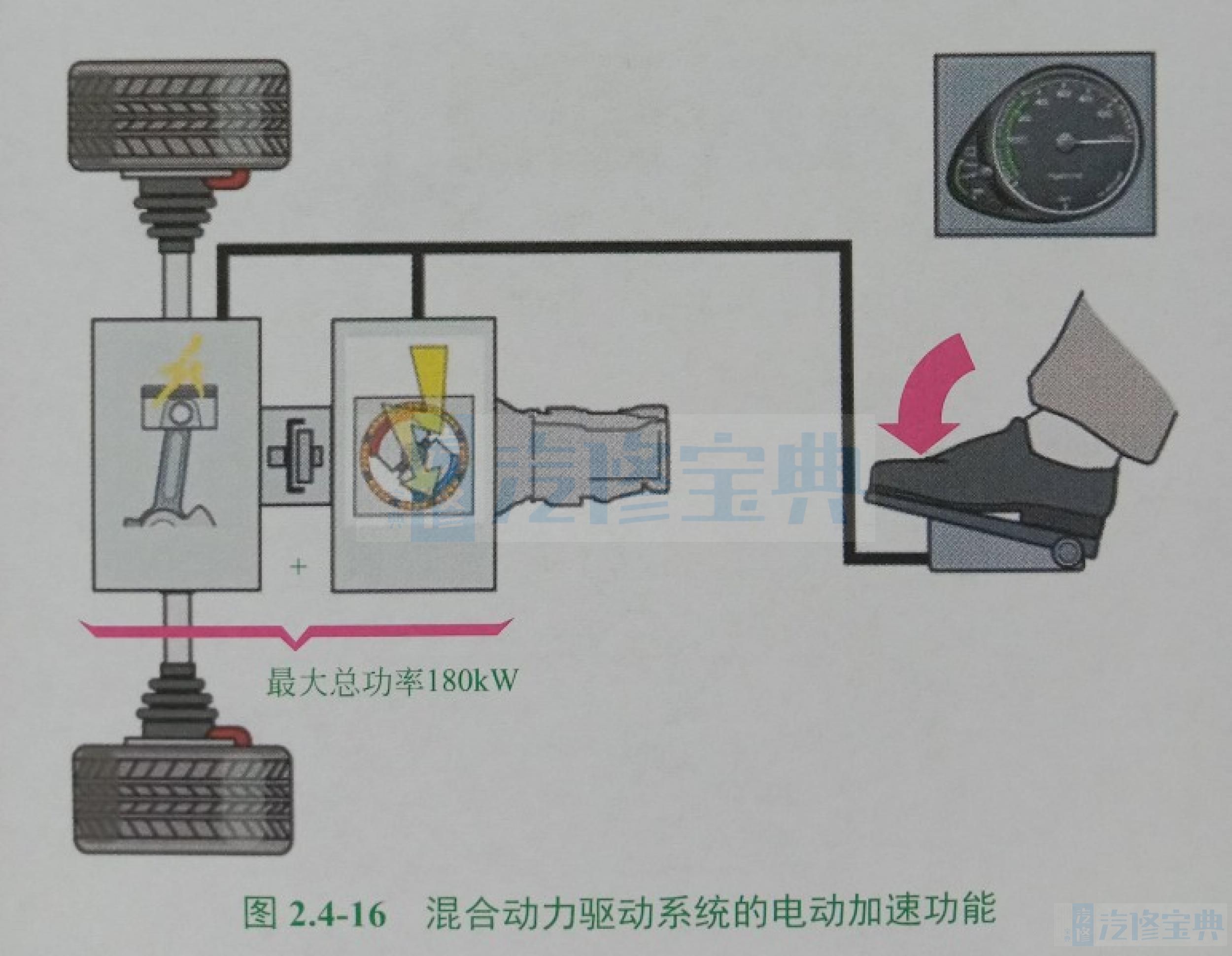
3.电动加速。
混合动力驱动系统有电动加速功能(图2.4-16),这与发动机的强制降挡功能(可提供最大发动机功率供使用)类似。如果执行了这个电动加速功能,那么电动机和内燃机就会发出最大功率(合计总功率很大)。这两种驱动方式各自功率合在一起,就是传动系统的总功率。
三、燃料电池汽车。
1.总体构造。
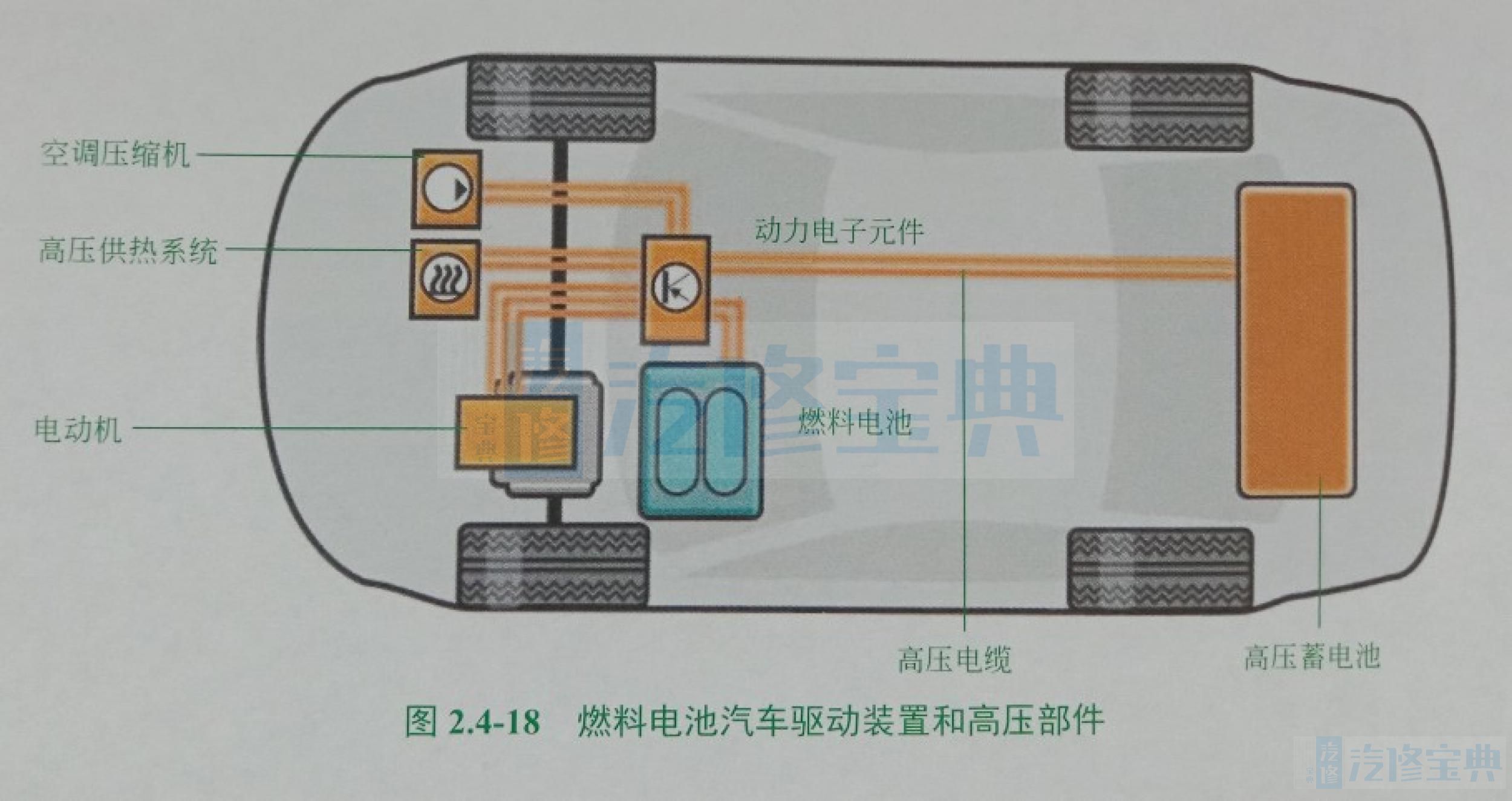
燃料电池汽车( FCBEV)采用燃料电池驱动(图2.4-17)。车辆以氢气作燃料,并从燃料电池模块为电动机获取电能。在该模块中,氢气转化为水以产生电能。根据操作模式,使用高压蓄电池的充电电压用于驱动(图2.4-18)。
在发动机中,通过燃烧将储存在燃料分子中的化学能转化为热能。由此产生的热能可用于驱动变速箱或供给交流发电机,这样,大量能量由于摩擦转化为热能。在燃料电池中,化学能转化为电能。与发动机不同,无需额外的交流发电机进行发电。
2.工作原理。
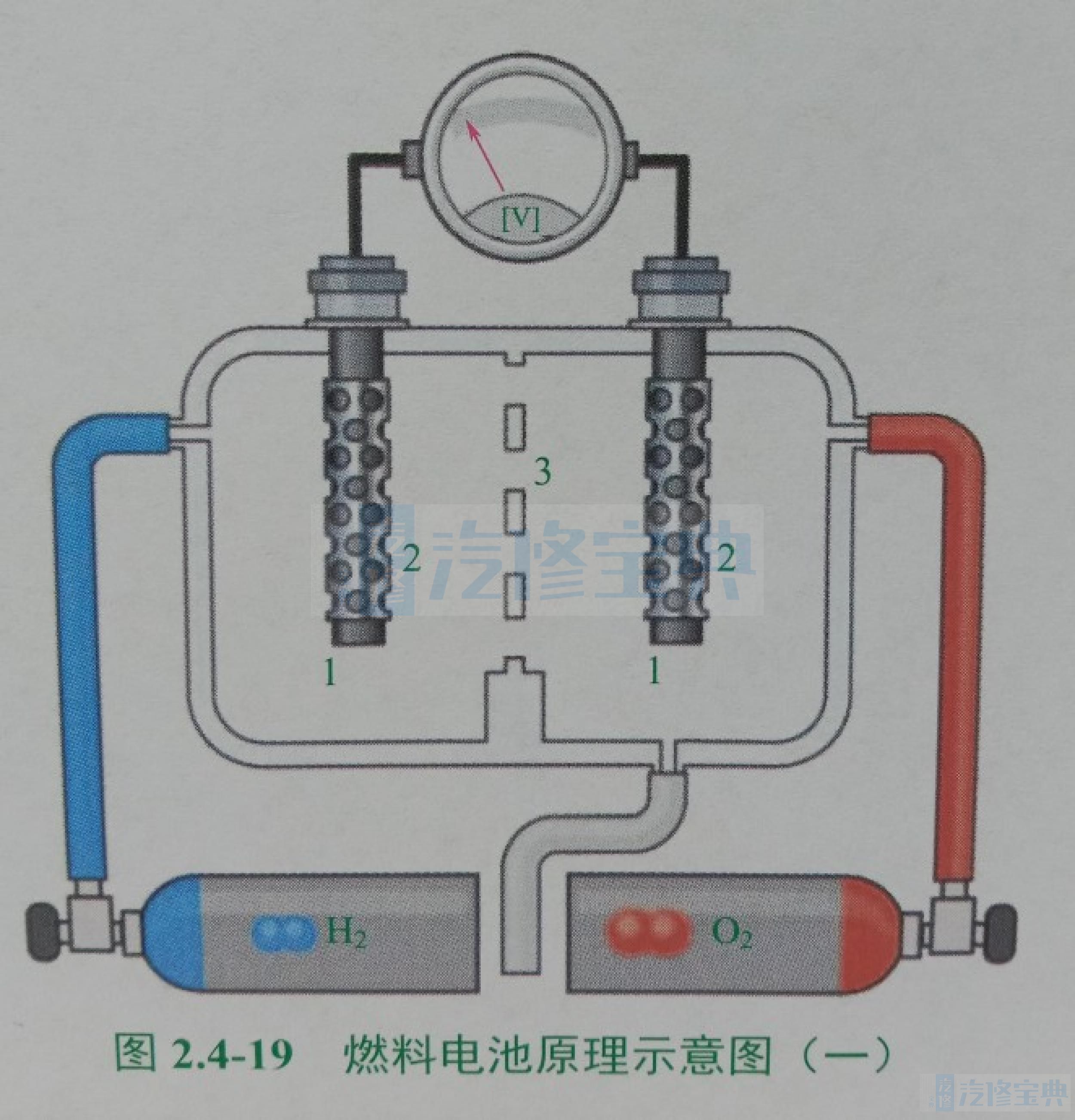
如图2.4-19所示,氢/氧燃料电池是原电池的一种特殊形式,主要部件为两个电极(1),镀铂的碳纤维纳米管用作催化剂(2)以及一层特殊薄膜(3)。多种化合物均可用作电极。
特殊薄膜具有气密性,对电子不导电,对质子(不带电子的氢核)具有渗透性。氧气(O 2)来自环境空气,无需专门填充。
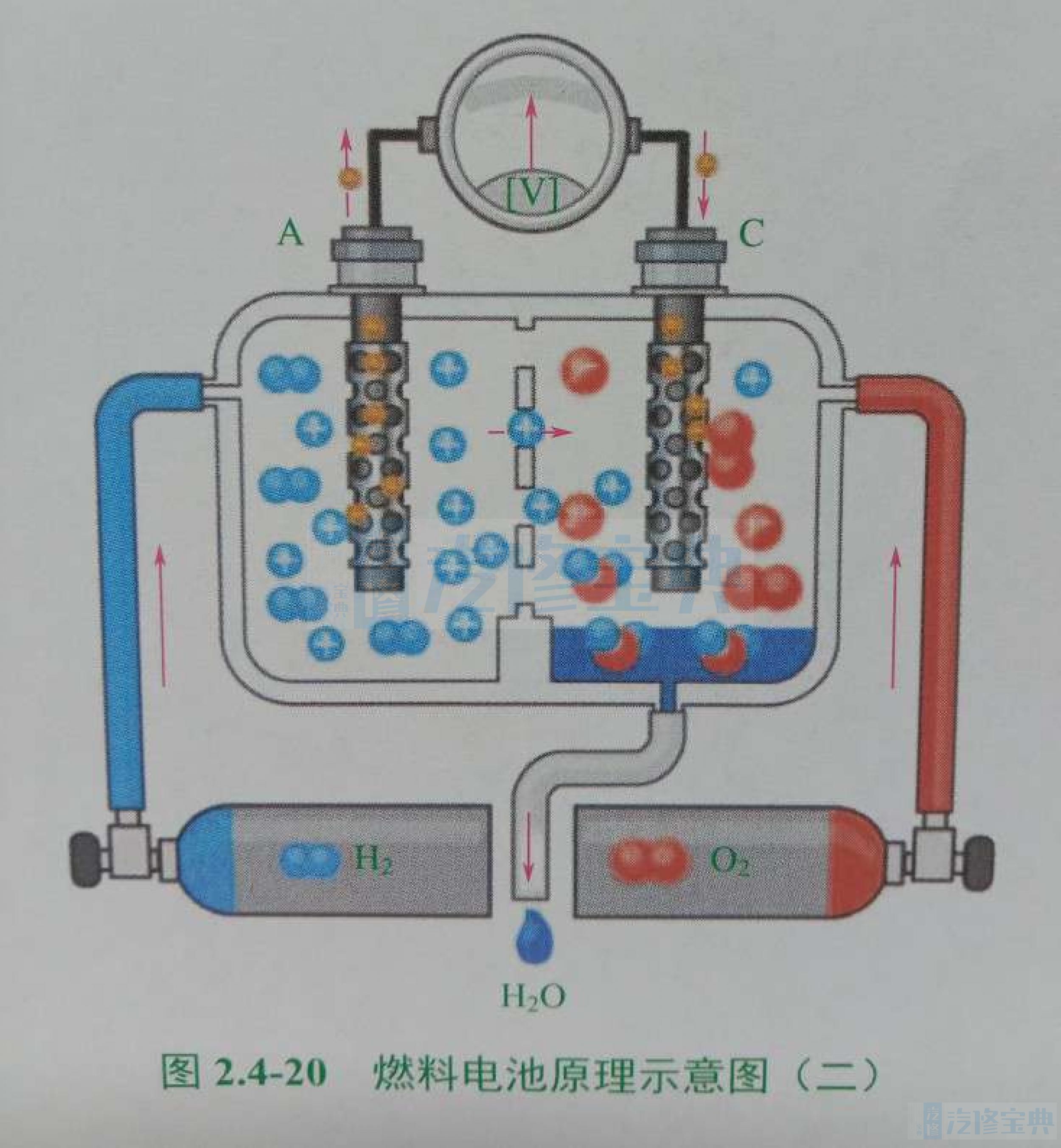
如图2.4-20所示,氢气(H2)和氧气(O2)分别分配至两个电极,氢气至正极(A),氧气至负极(C)。氢气在催化剂的作用下释放两个电子并分裂成两个带正电的氢核(质子)。
氢核可以渗入并穿过薄膜,因为薄膜另一侧(负极)电解质的质子数较正极少(扩散)。
氧气在其电极侧通过催化作用吸收电子,然后立即与自由的氢质子反应生成水(H2O)。于是,H2所具有的化学能便转变成了电能。